前編では、HER2陽性乳がん細胞の表面にHER2というタンパク質が多く存在する状態です。この特徴を持つがんは、特定の薬が効きやすいため、治療の選択肢が広がります。乳がんの治療の入口となる術前化学療法手術を行う前に、抗がん剤による薬物治療を先に実施する方法です。がんを事前に縮小させることで、手術を簡潔にしたり、生活の質を向上させたりする効果が期待できます。についてご説明しました。治療を受けた後、医師がもっとも重視する「病理学的完全奏効」という評価基準や、その結果に基づいた手術の選択肢、そして術後の治療方針の決まり方などが、本稿の重要なポイントです。
病理学的完全奏効(pCR)──治療の「成績表」を読む
術前化学療法を終えた後、いよいよ手術を行います。手術で摘出した組織は病理医の手によって詳細に調べられます。このとき最も注目されるのが、「病理学的完全奏効(pCR:pathological Complete Response)」を達成したかどうかという評価です。
pCRとは、術前化学療法の結果として、乳房のがん病巣と腋窩(わきの下)のリンパ節わきの下にあるリンパ節で、体の免疫機能に関わる重要な器官です。がんが転移しやすい場所であり、治療の判断に重要な役割を果たします。の両方から浸潤がん細胞正常な組織を破壊して周囲に広がるがん細胞のことです。非浸潤がんと異なり、進行性が高く、転移のリスクがあります。が完全に消失した状態を指します。わかりやすく言えば、「薬物治療でがん細胞をすべて壊すことができた」という最も良い反応です。
HER2陽性乳がんは、他のサブタイプと比較してpCRの達成率が高いことが知られています。トラスツズマブHER2陽性乳がんの治療に使う抗HER2薬で、商品名はハーセプチンです。HER2というタンパク質を標的として、がん細胞の成長を止めます。とペルツズマブトラスツズマブと同じく抗HER2薬の一種で、異なる仕組みでHER2に作用します。二つの抗HER2薬を組み合わせることで、治療効果が高まります。の二剤を使った抗HER2療法と化学療法の併用では、患者さんの特性(ホルモン受容体乳がん細胞の表面にある、女性ホルモン(エストロゲンやプロゲステロン)が結合する部分です。この受容体が陽性だと、ホルモン療法が効果的になります。の状態など)や使用するレジメン治療計画や投与スケジュールのことです。どの薬をどのくらいの量で、どのくらいの期間投与するかという具体的な治療内容を指します。によって異なりますが、試験データではおよそ40〜65%の方でpCRが得られています。これはHER2陽性乳がんが分子標的薬がん細胞に特有なタンパク質や遺伝子を狙い撃ちする薬です。正常な細胞への影響を少なくしながら、がん細胞を効率的に攻撃することができます。に対して高い感受性を持っていることの表れであり、治療の進歩を端的に示す数字でもあります。
pCRを達成できた場合は術後の再発リスクが非常に低いことが複数の大規模臨床試験で示されています。一方、pCRが達成されなかった場合(すなわち抗がん剤でがん細胞がすべて死滅していない状態:non-pCR術前化学療法後の手術で、がん細胞が完全には消えていない状態のことです。抗がん剤が完全に効き切らなかった部分があるため、術後の治療を強化する必要があります。)は、残念ながら再発リスクがやや高い傾向にあります。
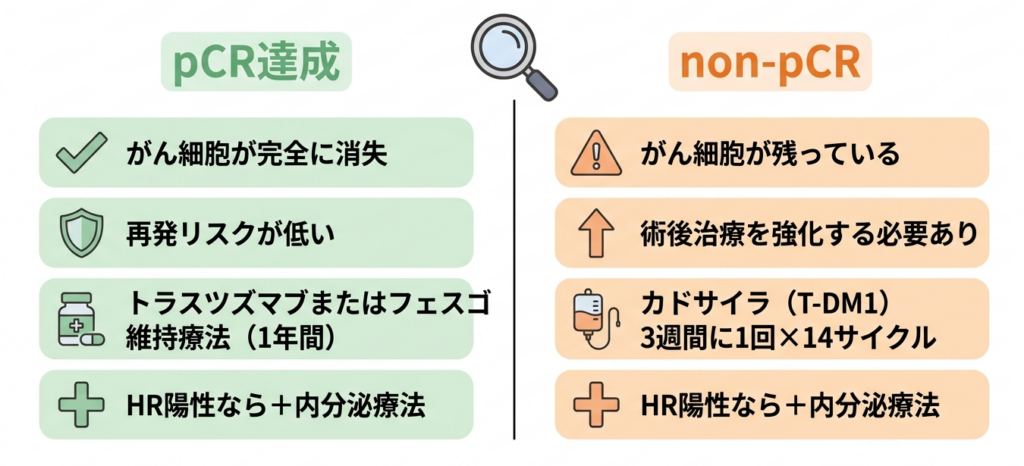
ここで重要なのは、pCRの達成・非達成によって術後補助療法の内容が変わるという点です。つまり、pCRの結果は単なる「成績表」にとどまらず、次に行う治療を決めるための極めて重要な判断材料になるのです。この考え方は「レスポンスガイド治療」と呼ばれ、HER2陽性乳がん治療における現代的なアプローチの核となっています。レスポンスとは治療への反応、すなわち治療効果のことですね。
手術の選択肢──乳房温存か乳房切除か
術前化学療法で腫瘍が十分に縮小した場合には、乳房温存手術(部分切除術)乳房全体ではなく、がんとその周辺の正常組織の一部だけを切除する手術です。乳房の形をある程度保つことができ、患者さんの生活の質向上につながります。を選択できる可能性が広がります。乳房温存手術は、がんとその周囲の正常組織を一部切除し、残った乳房に対して術後に放射線照射乳房温存手術後、残された乳房にがん細胞が再発するリスクを減らすため、放射線を照射する治療です。乳房温存手術とセットで行われることが標準的です。を行うというセットで完結します。乳房の形をある程度保つことができるため、患者さんの生活の質(QOL)にとって大きな意味があります。
一方で、腫瘍が大きい場合や乳房内に複数の病変がある場合、あるいはBRCA1やBRCA2といった遺伝子に病的バリアント(変異)乳がんや卵巣がんの発症リスクを高める遺伝子の異常のことです。この変異がある場合、両側の乳房にがんが発生するリスクが高いため、予防的に手術を考慮することがあります。がある場合には、乳房全切除術乳房全体を切除する手術です。腫瘍が大きい場合や複数ある場合、あるいは遺伝的リスクが高い場合に選択されることがあります。が推奨されることがあります。遺伝子変異がある方では、対側(反対側)の乳房にも将来がんが発生するリスクが高いため、リスク低減を目的として両側の乳房を切除するという選択肢についてもご相談することがあります。
乳房を全切除する場合でも、最近では乳房再建の技術が進歩しており、インプラント(人工乳房)乳房全切除後の再建に使う医療用の人工物です。シリコンなどでできており、外見を回復させるために手術で埋め込まれます。や自家組織患者さん自身のお腹や背中の皮膚や筋肉を使って、乳房を再建する方法です。人工物を使わないため、より自然な仕上がりが期待できます。(ご自身のお腹や背中の組織を使う方法)による再建手術を同時に、あるいは後日行うことが可能です。手術の方針は腫瘍の特性だけでなく、患者さんの希望や体格、既往歴なども総合して決定されますので、担当医としっかり話し合うことが大切です。
術後補助療法①──pCRを達成できた場合
手術検体の病理検査でpCRが確認された場合、術後には抗HER2薬の維持療法を行います。具体的には、トラスツズマブ(ハーセプチン)もしくはフェスゴ(ペルツズマブ+トラスツズマブの合剤)を、術前に開始した時期から数えて合計1年間となるよう継続します。3週間に1回のペースで点滴あるいは皮下注射を行い、おおむね手術後の約9か月間がこの維持療法の期間に相当します。
pCRを達成した患者さんは、術前化学療法が十分に効いたということですから、術後はシンプルな抗HER2薬の維持で再発リスクを低く抑えることを目指すわけです。
なお、腫瘍が小さく(T1)リンパ節転移もない患者さんで、手術を先行させた場合には、APT試験のデータに基づいたパクリタキセル植物由来の抗がん剤で、細胞分裂を止めることでがん細胞を殺します。アントラサイクリン系薬に比べて心臓への負担が少ないという利点があります。+トラスツズマブ(アントラサイクリン系抗がん剤強力な抗がん剤のグループで、多くの抗がん剤治療で使われます。効果が高い一方で、心臓への負担が比較的大きいという課題があります。を使わない方法)が術後補助療法として選択されることがあります。心臓への負担を軽減でき、抗がん剤治療の期間を短くすることが利点です。どのアプローチが適切かは腫瘍の特性に応じて担当医が判断します。
ここでもう一つ確認しておきたいのが、ホルモン受容体の状態です。HER2陽性乳がんの中には、ホルモン受容体(エストロゲン受容体やプロゲステロン受容体)も同時に陽性である「HER2陽性かつHR陽性」というタイプが一定数存在します。このタイプの場合、抗HER2薬の維持療法と並行して内分泌療法(ホルモン療法)ホルモン受容体陽性の乳がんに対して、女性ホルモンの働きを抑えたり、ホルモンの受け取りを遮断したりする治療です。数年間の長期投与が効果的です。も行います。
内分泌療法の内容は、閉経前か閉経後かで異なります。閉経後の方にはアロマターゼ阻害薬閉経後の女性に使うホルモン療法の薬です。エストロゲンを作る酵素(アロマターゼ)の働きを阻害し、体内のホルモン量を低下させます。が使われることが多く、閉経前の方にはタモキシフェン閉経前の女性に主に使うホルモン療法の薬です。乳がん細胞がエストロゲンを受け取るのをブロックすることで、がんの成長を抑えます。が基本となりますが、リスクに応じてLH-RHアゴニスト卵巣の機能を一時的に抑制する注射薬で、閉経前の女性のホルモン療法に使われます。特にリスクが高い患者さんでホルモン療法の効果を高めるために併用されます。(卵巣機能を抑制する注射薬)を使うこともあります。内分泌療法は通常5年間、場合によってはさらに延長して10年間継続することが推奨されており、抗HER2薬の1年間が終わった後もホルモン療法は続くことになります。
この「抗HER2薬+内分泌療法」の二本柱が、HER2陽性かつHR陽性の方にとっての術後治療の基本形です。
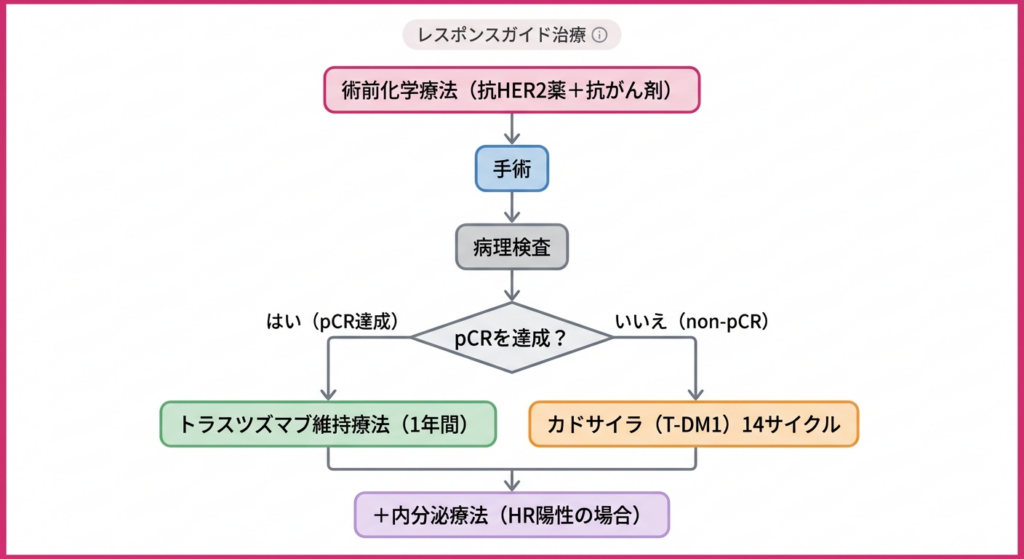
術後補助療法②──pCRが達成されなかった場合(non-pCR)
術前化学療法を行ったにもかかわらず、手術で摘出した組織の中にがん細胞が残っていた場合を「non-pCR」と呼びます。がん細胞が残っていたという事実は、術前に使った抗がん剤が完全にがん細胞を殺しきれなかった部分があったことを意味しますので、術後の治療を強化する必要があります。
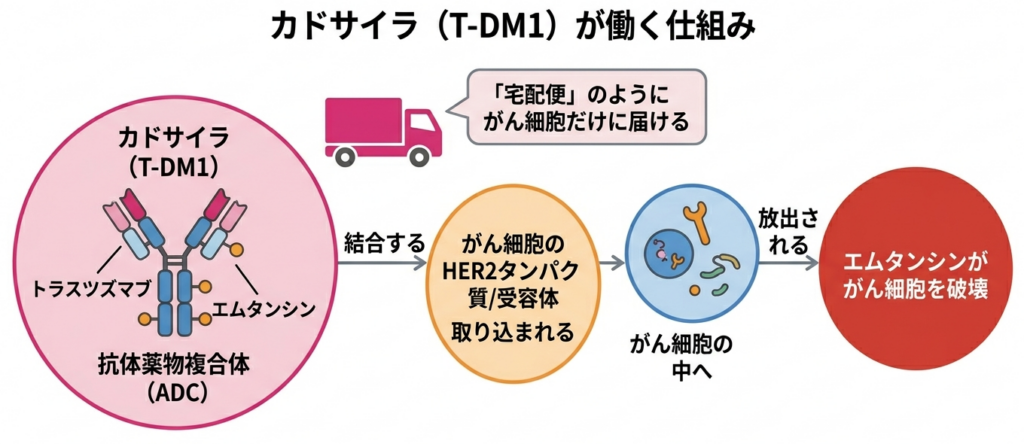
このnon-pCRの方に対して現在推奨されているのが、カドサイラ(トラスツズマブ エムタンシン:T-DM1)抗HER2抗体と強力な抗がん剤を組み合わせた新しいタイプの薬です。がん細胞だけを選別して攻撃するため、正常な細胞への影響を抑えることができます。という薬剤です。カドサイラは、抗HER2抗体であるトラスツズマブと、エムタンシンという強力な抗がん剤を化学的に結合させた「抗体薬物複合体(ADC:Antibody-Drug Conjugate)」と呼ばれるタイプの薬です。
カドサイラがどのように働くかというと、まずトラスツズマブの部分ががん細胞表面のHER2タンパク質に結合し、薬剤ががん細胞の中に取り込まれます。すると細胞内でエムタンシンが放出され、がん細胞を内側から破壊します。いわば「宅配便」のように、がん細胞だけに薬を届けて効かせる仕組みであり、正常な細胞への影響を相対的に抑えることができるのが特徴です。
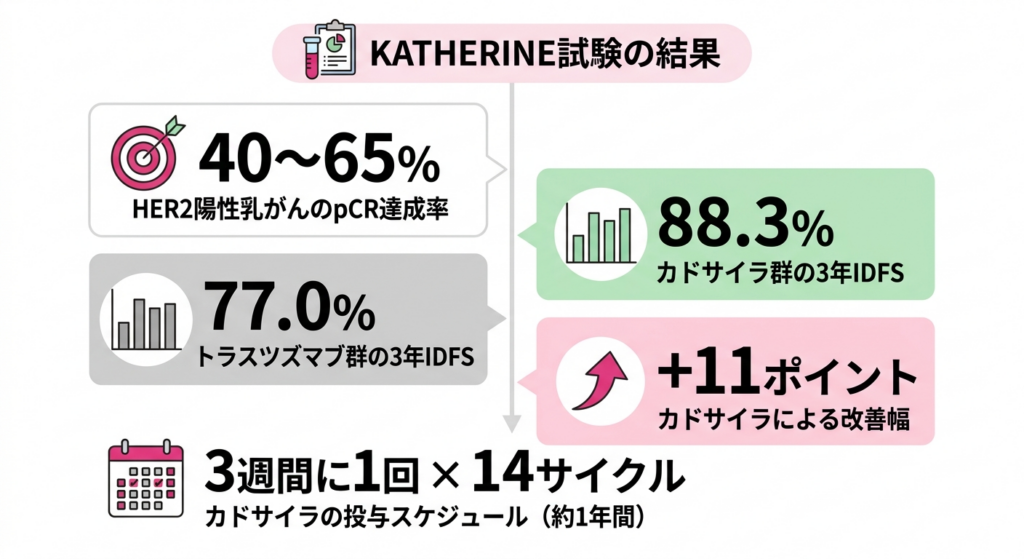
カドサイラの有効性を確立した臨床試験がKATHERINE試験術前化学療法後にがん細胞が残った患者さんを対象に、カドサイラの効果を調べた大規模な臨床試験です。この試験の結果、カドサイラが標準治療として採用されるようになりました。です。この試験では、術前化学療法後にnon-pCRだった患者さんを対象に、術後にT-DM1を投与するグループと、従来どおりトラスツズマブ単剤を投与するグループを比較しました。
その結果、カドサイラのグループでは侵襲性疾患フリー生存率がんが再発したり、新たな浸潤がんが発生したりせず、生存している患者さんの割合を示す指標です。治療の効果を評価する重要な数字です。(再発や新たな浸潤がんの発生なく生存している割合)が有意に改善しました。3年時点での浸潤癌の再発が発生しない生存率(IDFS)はT-DM1群で88.3%、トラスツズマブ群で77.0%と、約11ポイントの絶対的な差が示されています。この結果は非常にインパクトが大きく、KATHERINE試験以降、non-pCR例に対するカドサイラの使用は世界的に標準治療として定着しました。
カドサイラは3週間に1回の点滴で投与され、14サイクル(約1年間)にわたって継続されます。投与中は肝機能や血小板数などの血液検査を定期的に行い、副作用の管理を丁寧に行いながら進めていきます。
non-pCRの方でHER2陽性かつHR陽性の場合は、カドサイラと並行して内分泌療法も行います。カドサイラの1年間が終了した後も内分泌療法は引き続き継続となりますので、この点はpCR達成例と同じ考え方です。
術前化学療法の成果を確認し、手術を無事に終えた後も、HER2陽性乳がんの治療は続きます。特にpCRが達成されなかった患者さんや、ホルモン受容体陽性の患者さんに対しては、さらに治療法が加わります。後編では、その先の治療と、長期の付き合い方についてお話しします。
📖 乳がんサブタイプ別の最新治療 〜 初期治療編(8/10)
