乳がん診療ニュース
エンハーツが術前治療でも有効性を示した ── DESTINY-Breast11試験の結果を読み解く
抗体薬物複合体が切り拓いてきた道のり
HER2タンパクを標的とした治療の歴史は、1998年にトラスツズマブ(ハーセプチン)が米国で承認されたことに始まります。それまでHER2陽性乳がんは予後の厳しいタイプとして知られていましたが、トラスツズマブの登場によって治療成績は劇的に改善しました。その後、ペルツズマブやT-DM1といった薬剤が次々と開発され、HER2陽性乳がんの治療は着実に進歩してきました。
そして2020年代に入り、新たな抗体薬物複合体(抗体と抗がん剤を結合させた薬)であるトラスツズマブ デルクステカン、商品名エンハーツ(T-DXd)が、転移・再発乳がんの領域ですぐれた治療成績を示し、世界中の治療指針に影響を与えています。
そのエンハーツが、今度は「手術の前に行う薬物治療」、いわゆる術前化学療法の領域でも有効性を証明しました。DESTINY-Breast11試験と呼ばれるこの大規模な国際共同試験の結果が、腫瘍学の権威ある学術誌Annals of Oncology誌に掲載されたのです。
本記事では、HER2陽性乳がんと診断された患者さんに向けて、この試験結果がどのような意味を持つのかをわかりやすく解説していきます。
術前化学療法とは何か、なぜ行うのか
手術の前に薬物治療を行うことを術前化学療法(ネオアジュバント療法)と呼びます。目的はいくつかありますが、特に大きいのは、薬の力でがんを小さくしてから手術を行うことで、切除範囲を最小限に抑えられる可能性があるという点です。もともと乳房全摘が必要と考えられていた方でも、がんが十分に縮小すれば乳房温存手術が可能になることがあります。
治療効果の指標として重視されるのが「pCR(病理学的完全奏効)」です。これは、術前治療のあとに手術で取り出した組織を顕微鏡で詳しく調べたとき、がん細胞がまったく残っていない状態を指します。pCRが得られた患者さんは、得られなかった患者さんと比べて再発リスクが低いことが多くの研究で示されており、術前治療の「通信簿」のような役割を果たしています。HER2陽性乳がんの治療全体については、当サイトの解説記事「HER2陽性乳がんの治療」もあわせてご覧ください。
いま標準とされている術前レジメン
現在、HER2陽性早期乳がんに対する術前化学療法の標準的なレジメンは「アンスラサイクリン→抗HER2薬を含む抗がん剤」です。前半では、アンスラサイクリン系と呼ばれる抗がん剤であるドキソルビシンやエピルビシンとシクロホスファミドの2剤を、2週間ごとに計4回投与します。後半では、タキサン系抗がん剤に加え、トラスツズマブとペルツズマブという2種類の抗HER2薬を組み合わせて投与します。
このレジメンによるpCR率はおよそ50〜60%と報告されており、半数以上の方でがん細胞の完全消失が期待できます。ただし課題もあります。前半に使うアンスラサイクリン系薬剤には心臓への毒性(心毒性)があり、長期的に心機能が低下するリスクが知られています。
また、白血球が著しく減少する骨髄抑制も強く、治療中の感染症リスクや体力の消耗に悩む方が少なくありません。「もっと効果が高く、かつ体への負担が少ないレジメンがあれば」というのは、患者さんも医療者も共通して抱いてきた願いです。
DESTINY-Breast11試験はどのように設計されたか
DESTINY-Breast11試験は、腫瘍径が5cmを超える、あるいはリンパ節転移が認められるハイリスクのHER2陽性乳がんの患者さんを対象とした国際共同第III相試験です。18カ国・147施設が参加しており、信頼性の高い大規模試験として設計されました。
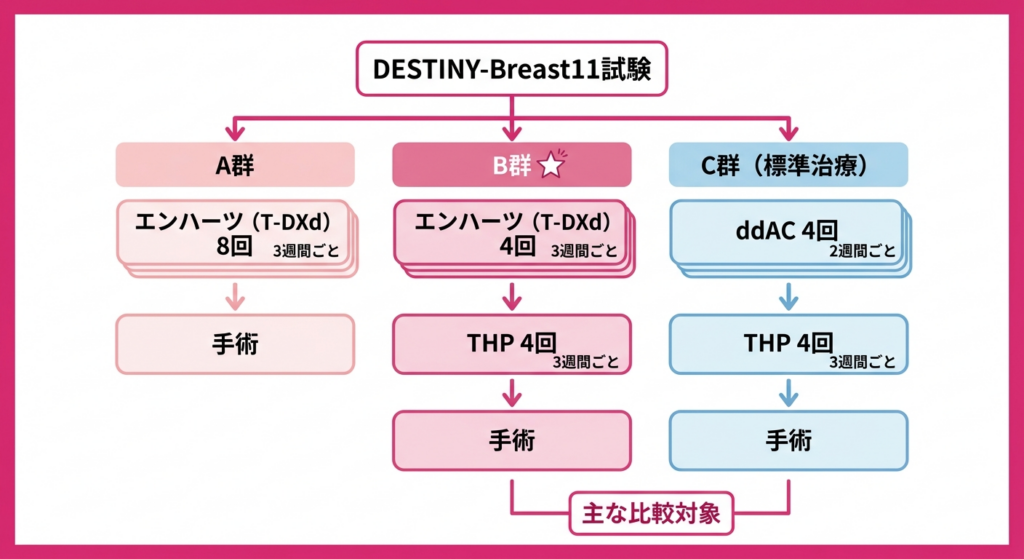
この試験では、参加者を3つの治療群に振り分けて比較しています。A群はエンハーツ単独を3週間ごとに8回投与したあとに手術を行う群、B群はエンハーツを4回投与してからTHP(パクリタキセル+トラスツズマブ+ペルツズマブ)を4回投与し手術に進む群、そしてC群は従来の標準治療であるアンスラサイクリン4回投与のあとにTHP4回を行って手術に進む群です。
試験の最も重要な比較対象はB群とC群、つまり「エンハーツを組み込み、アンスラサイクリンを使わないレジメン」と「従来のアンスラサイクリンを含む標準レジメン」の直接比較でした。強力だけれども体への負担が大きいアンスラサイクリンを使わずに、同等以上の治療効果が得られるのかどうか。これが試験の核心です。
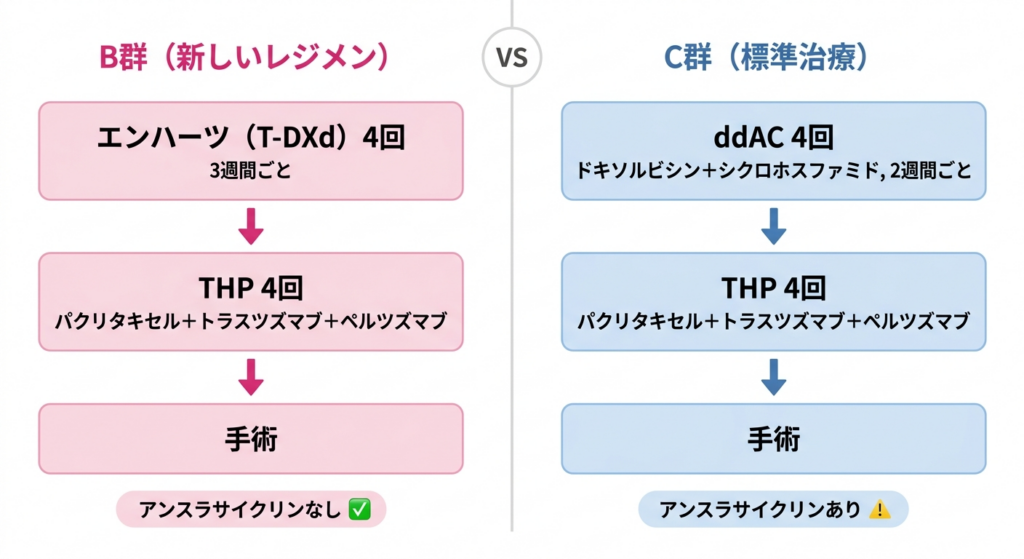
効果も副作用も、ともに改善という結果
結果は期待を上回るものでした。pCR率を見ると、B群(エンハーツ+THP)が67.3%、C群(標準治療)が56.3%で、B群が約11ポイント上回りました。この差は統計学的にも有意であり、偶然とは考えにくい明確な差です。わかりやすくいえば、100人の患者さんがいたとして、従来の治療では約56人にがん細胞の完全消失が見られるところ、新しいレジメンでは約67人に達するということです。約11人多くの方で、手術時にがん細胞が見つからない状態が実現したことになります。
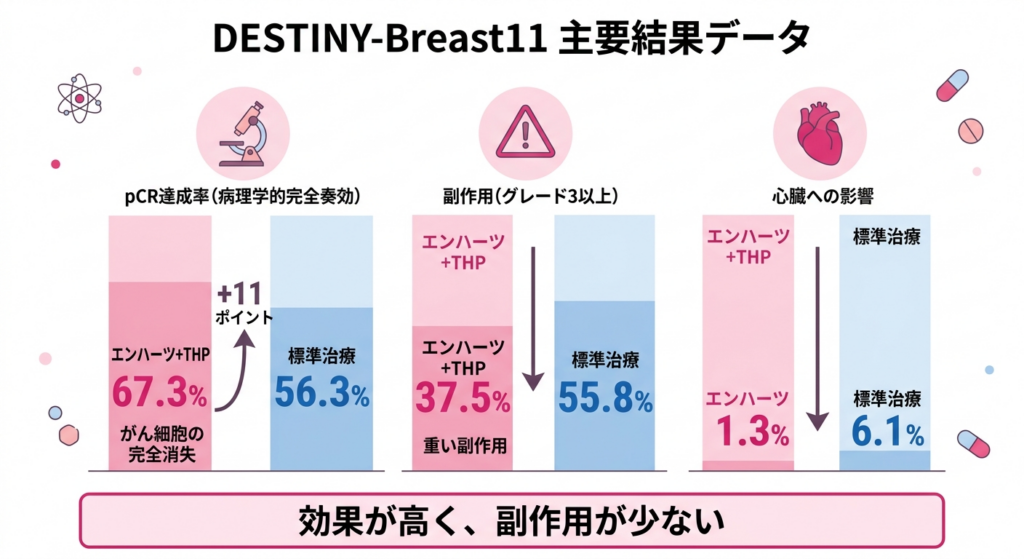
さらに注目すべきは副作用の軽減です。重い副作用(グレード3以上、つまり入院や積極的な治療介入が必要な水準のもの)の発生率は、B群が37.5%に対してC群が55.8%でした。心臓への影響に限ると、B群はわずか1.3%であったのに対し、C群では6.1%と報告されています。重篤な副作用全体で見ても、B群が10.6%、C群が20.2%と、ほぼ半分の水準にとどまりました。
この結果が画期的である理由は、「アンスラサイクリンを使わないにもかかわらず治療効果が上がり、しかも副作用が軽くなった」という、従来の常識を覆す二重の改善が示されたことにあります。患者さんの中には、「効果を上げるには副作用も覚悟しないといけないのでは」と考えている方が多いのですが、今回の試験は、その「効果と副作用は引き換え」という構図を変える可能性を示してくれました。
今後の見通しと患者さんに知っておいていただきたいこと
現時点では、エンハーツを術前治療として使用することは日本ではまだ承認されていません。ただし、世界では承認に向けた動きが急速に進んでいます。
米国では2025年10月に食品医薬品局(FDA)が承認申請を受理しており、審査期限は2026年5月18日に設定されています。中国では2026年3月に、世界で初めてこの術前適応について条件付き承認が下りました(長期的な有効性の確認が承認継続の条件とされています)。
日本では、エンハーツの術後適応(手術後に病変が残った場合の治療)について2026年2月にPMDA(医薬品医療機器総合機構)へ承認申請が出されていますが、術前適応についてはまだ申請されていません。したがって、日本で実際に使えるようになるまでにはもう少し時間がかかる見込みです。
振り返ると、エンハーツの適応は段階的に広がってきました。最初は転移・再発乳がんの治療薬として承認され、その後、手術後に病変が残っていた患者さんに対する術後補助療法としても成果を示しています(「エンハーツ術後療法のFDA優先審査について」)。そして今回、術前治療という新たなステージでも有効性が確認されたわけです。がんとの闘いにおいてエンハーツが担う役割は、着実に拡大しています。
まとめ
DESTINY-Breast11試験は、エンハーツを含みアンスラサイクリンを使わない術前レジメンが、従来の標準治療と比較してpCR率を約11ポイント改善し、同時に重篤な副作用を大幅に減少させたことを示しました。「より高い効果」と「より少ない副作用」の両立は、HER2陽性早期乳がんの術前治療における新たな標準となる可能性があります。
今後は承認審査の進展とともに、長期的な再発予防効果のデータが蓄積されていく段階です。本試験の結果は、近い将来の治療選択肢を広げる重要な科学的根拠といえるでしょう。
出典: 本記事は、Annals of Oncology誌に掲載されたDESTINY-Breast11試験の結果、およびESMO 2025での発表データに基づいています。
